出国留学网专题频道药事管理与法规复习资料栏目,提供与药事管理与法规复习资料相关的所有资讯,希望我们所做的能让您感到满意!
11-25
考试临近,出国留学网定期为你整理执业药师复习要点,与你一起巩固知识点,更多执业药师考试资讯,网站将持续更新,敬请关注!
2017年《药事管理与法规》考点:野生药材资源保护管理
国务院发布《野生药材资源保护管理条例》
一、《野生药材资源保护管理条例》的适用范围和原则
适用范围:在我国境内采猎、经营野生药材的任何单位和个人。
原则:国家对野生药材资源实行保护、采猎相结合的原则,并创造条件开展人工种养。
二、国家重点保护的野生药材物种的三级管理
一级【濒危稀有物种】保护野生药材物种-指濒临灭绝状态的稀有珍贵野生药材物种。
包括4种:(虎骨)、豹骨、羚羊角、鹿茸(梅花鹿)。
二级【衰竭重要物种】保护野生药材物种-指分布区域缩小,资源处于衰竭状态的重要野生药材物种;
包括17种:鹿茸(马鹿)、麝香、熊胆、穿山甲、蟾酥、蛤蟆油、金钱白花蛇、乌梢蛇、蕲蛇、蛤蚧、甘草、黄连、人参、杜仲、厚朴、黄柏、血竭。
【①马②草射蟾③二黄④双蛤⑤穿厚杜⑥三蛇⑦熊人血⑧虎豹羚羊梅花鹿】
注:①马:马鹿茸。②草射蟾:甘草、麝香、蟾酥。③二黄:黄连、黄柏。④双蛤:蛤蚧、蛤蟆油。⑤穿厚杜:穿山甲片、厚朴、杜仲。⑥三蛇:蕲蛇、乌梢蛇、金钱白花蛇。⑦熊人血:人参、熊胆、血竭。⑧虎豹羚羊梅花鹿:指4种一级保护野生药材品种虎骨、豹骨、羚羊角、梅花鹿茸。
三级【严重减少常用物种】保护野生药材物种-指资源严重减少的主要常用野生药材物种。
包括22种:川贝母、伊贝母、刺五加、黄芩、天冬、猪苓、龙胆、防风、远志、胡黄连、肉苁蓉、秦艽、细辛、紫草、五味子、蔓荆子、诃子、山茱萸、石斛、阿魏、连翘、羌活。
【①紫薇丰萸②猪肉③川味黄连④荆诃刺秦⑤远东⑤远东⑥胆⑦细⑧活】
注:①紫薇丰萸:紫草、阿魏、防风、山茱萸。②猪肉:猪苓、肉苁蓉。③川味黄连:川(伊)贝母、五味子、胡黄连、黄芩、连翘。④荆诃刺秦:蔓荆子、诃子、刺五加、秦艽。⑤远东:远志、天冬。⑥胆:龙胆(草)。⑦细:细辛。⑧活:羌活。
三、国家重点保护的野生药材的采猎、出口管理规定
1.对一级保护野生药材物种的管理【禁止采猎、不得出口】:
禁止采猎一级保护野生药材物种。一级保护野生药材物种属于自然淘汰的,其药用部分由各级药材公司负责经营管理,但不得出口。
2.对二、三级保护野生药材物种的管理【计划采收、限量出口】:
采购、收购二、三级保护野生药材物种必须按照批准的计划进行。采猎者必须持有采药证,需进行采伐或狩...
11-24
考试临近,出国留学网定期为你整理执业药师复习要点,与你一起巩固知识点,更多执业药师考试资讯,网站将持续更新,敬请关注!
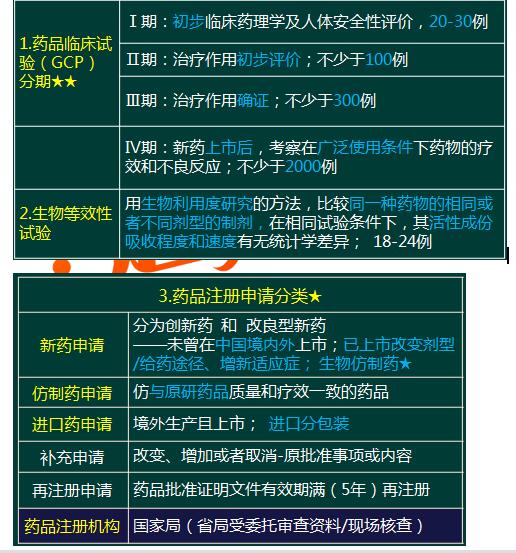
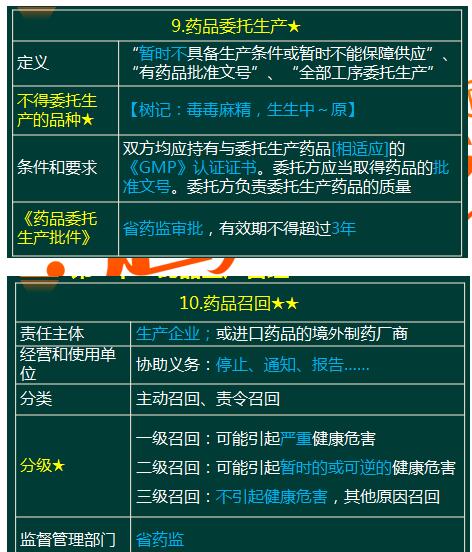
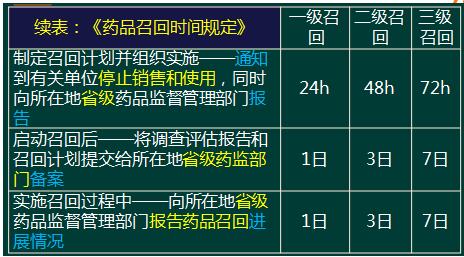
2017年《药事管理与法规》考点:药品研制与生产管理



出国留学网执业药师栏目推荐:
11-15
考试临近,出国留学网定期为你整理执业药师复习要点,与你一起巩固知识点,更多执业药师考试资讯,网站将持续更新,敬请关注!
2017年《药事管理与法规》考点:药品安全法律责任
(一)药品安全法律责任与特征
(1)药品安全法律责任:是指由于违反药品法律法规所应承担的法律后果,包括四大构成要件:
以存在违法行为为前提
有法律明文规定违法行为所应承担的不利后果
有国家强制力保证执行
由专门机关追究法律责任
(2)药品安全法律责任的种类
刑事责任(如生产、销售假药罪,生产、销售劣药罪,非法提供麻醉药品、精神药品罪等)
民事责任(人身伤害、财产损失,诉讼时效期间为两年)
行政责任(行政处罚和行政处分)。
(二)生产、销售假药、劣药的法律责任
(1)假药的认定:禁止生产、销售假药
有下列情形之一的,为假药:①药品所含成份与国家药品标准规定的成份不符的;②以非药品冒充药品或者以他种药品冒充此种药品的。
有下列情形之一的药品,按假药论处:①国务院药品监督管理部门规定禁止使用的;②依照本法必须批准而未经批准生产、进口,或者依照本法必须检验而未经检验即销售的;③变质的;④被污染的;⑤使用依照本法必须取得批准文号而未取得批准文号的原料药生产的;⑥所标明的适应症或者功能主治超出规定范围的。
擅自委托或者接受委托生产药品的,对委托方和受托方均依照生产、销售假药的法律责任给予处罚。
(2)生产、销售假药的行政责任
1.单位承担的行政责任:生产、销售假药的,没收违法生产、销售的药品和违法所得,并处违法生产、销售药品货值金额二倍以上五倍以下的罚款;有药品批准证明文件的予以撤销,并责令停产、停业整顿;情节严重的,吊销《药品生产许可证》、《药品经营许可证》或者《医疗机构制剂许可证》。
2.相关人员承担的行政责任:从事生产、销售假药的企业或者其他单位,其直接负责的主管人员和其他直接责任人员十年内不得从事药品生产、经营活动。
3.从重处罚的情节:生产、销售假药(劣药),有下列行为之一的,从重处罚:
①以麻醉药品、精神药品、医疗用毒性药品、放射性药品冒充其他药品,或者以其他药品冒充上述药品的;
②生产、销售以孕产妇、婴幼儿及儿童为主要使用对象的假药的;
③生产、销售的生物制品、血液制品属于假药的;
④生产、销售假药,造成人员伤害后果的;
⑤生产、销售假药,经处理后重犯的;
⑥拒绝、逃避监督检査,或者伪造、销毁、隐匿有关证据材料的,或者擅自动用查封、扣押物品的。
(3)生产、销售假药的刑事责任
《刑法》第141条规定,生产、...
11-15
考试临近,出国留学网定期为你整理执业药师复习要点,与你一起巩固知识点,更多执业药师考试资讯,网站将持续更新,敬请关注!
2017年《药事管理与法规》考点:医疗器械、保健食品和化妆品的管理
(一)医疗器械管理
1.医疗器械管理的基本要求
(1)医疗器械的界定:是指直接或者间接 用于人体的仪器、设备、器具、体外诊断试剂及校准物、材料以及其他类似或者相关的物品,包括所需要的计算机软件;其效用主要通过物理等方式获得 ,不是通过药理学、免疫学或者代谢的方式获得,或者虽然有这些方式参与但是只起辅助作用 ;
其目的是:①疾病 的诊断、预防、监护、治疗或者缓解;②损伤 的诊断、监护、治疗、缓解或者功能补偿;③生理 结构或者生理过程的检验、替代、调节或者支持;④生命 的支持或者维持;⑤妊娠 控制;⑥通过对来自人体的样本进行检查 ,为医疗或者诊断目的提供信息。
(2)医疗器械的分类
国家对医疗器械按照风险程度实行分类管理。评价医疗器械风险程度,应当考虑医疗器械的预期目的、结构特征、使用方法等因素。
第一类是风险程度低,实行常规管理 可以保证其安全、有效的医疗器械。
如外科用手术器械(刀、剪、钳、镊夹、针、钩)、听诊器(无电能)、反光镜、反光灯、医用放大镜、(中医用)刮痧板、橡皮膏、透气胶带、手术衣、手术帽、检查手套、集液袋等。
第二类是具有中度风险,需要严格控制管理以保证其安全、有效 的医疗器械。
如血压计、体温计、心电图机、脑电图机、手术显微镜、(中医用)针灸针、助听器、皮肤缝合钉、避孕套、避孕帽、无菌医用手套、睡眠监护系统软件、超声三维系统软件、脉象仪软件等。
第三类是具有较高风险,需要采取特别措施严格控制管理 以保证其安全、有效的医疗器械。
如心脏起搏器、体外反搏装置、血管内窥镜、超声肿瘤聚焦刀、高频电刀、微波手术刀、医用磁共振成像设备、钴60治疗机、正电子发射断层扫描装置(PECT)、植入器材、植入式人工器官、血管支架、血管内导管、一次性使用输液器、输血器等。
(3)产品注册与备案管理
第一类医疗器械实行备案管理。第二类、第三类医疗器械实行注册管理。
境内第一类 医疗器械备案,备案人向设区的市级药品监督管理部门 提交备案资料。境内第二类 医疗器械由省级药品监督管理部门 审查,批准后发给医疗器械注册证。境内第三类 医疗器械由国家药品监督管理部门审査 ,批准后发给医疗器械注册证。
进口第一类 医疗器械备案,备案人向国家药品监督管理部门 提交备案资料。进口第二类、第三类 医疗器械由国家药品监督管理部门审查 ,批准后发给医疗器械注册证。
香港、澳门、台湾地区医疗器械的注册、备案,参照进口医疗器械办理。
境内生产的医疗器械,应当由境内申请人(备案人)申请注册或者办理备案。
进口医疗器械,应当由境外申请人(备案人)作为注册...
11-13
考试临近,出国留学网定期为你整理执业药师复习要点,与你一起巩固知识点,更多执业药师考试资讯,网站将持续更新,敬请关注!
2017年《药事管理与法规》考点:专有、专用标识
1、麻醉药品、精神药品、医疗用毒性药品、放射性药品、外用药品和非处方药的标签,必须印有规定的标志。
2、OTC的标签、使用说明书、内包装、外包装必须印有OTC专有标识(一体化印刷,右上角)。红色:甲类;绿色:乙类、企业指南性标志。
2、疫苗生产企业、批发企业供应的纳入国家免疫规划疫苗的最小外包装的显著位置:标明“免费”字样、国务院卫生行政主管部门规定的“免疫规划”专用标识。
3、互联网网站标注
(1)提供互联网药品交易服务的企业网站首页显著位置标明:互联网药品交易服务机构资格证书号码。
(2)提供互联网药品信息服务的网站,应当在其网站主页显著位置标注《互联网药品信息服务资格证书》的证书编号。
4、按医疗用毒性药品管理的药材及其饮片制成的单方制剂,必须标注:医疗用毒性药品标识。
5、外用药品标识的要求
A红色方框底色内标注白色“外”字
B应当彩色印刷的:药品标签中
C可以单色印刷:说明书中
D需标注外用药品标识的情况:国家标准中用法项下规定只可外用,不可口服、注射、滴入或吸入,仅用于体表或某些特定粘膜部位的液体、半固体或固体中药、天然药物
E可不标注外用药品标识的情况:既可内服,又可外用的中药、天然药物
6、标注位置总结
右上角:
A. OTC专有标识在标签、使用说明书、内包装、外包装右上角。
B. 急诊处方,在右上角标注“急诊”
C. 儿科处方,在右上角标注“儿科”
D. 麻醉、精一,在右上角标注“麻”、“精一”
E. 精二,在右上角标注 “精二”
右上方:麻醉药品、精神药品、医疗用毒性药品、放射性药品、外用药品专用标识。中药饮片处方调剂、煎煮的特殊要求注明在药品的右上方
左上角:药品说明书的核准和修改日期,修改日期位于核准日期下方,按时间顺序逐行书写(注意中药、天然药物和化学药、生物药有点不同,修改多次日期的,仅列最后一次)
药品说明书上方:“请仔细阅读说明书并在医师指导下使用”
7、颜色总结
白色:普通、精二处方印刷用纸
淡黄色:急诊处方印刷用纸
黄色:药品批发和零售连锁待验药品库(区)、退货药品库(区)
淡绿色:儿科处方印刷用纸
绿色:乙类OTC、经营非处方药药品的企业指南性标志、药品批发和零售连锁合格药品库(区)、零货称取库(区)、待发药品库(区)
淡红色...
11-13
考试临近,出国留学网定期为你整理执业药师复习要点,与你一起巩固知识点,更多执业药师考试资讯,网站将持续更新,敬请关注!
2017年《药事管理与法规》考点:使用药品时有关记录
1、处方前记:医疗机构名称、费别、患者姓名、性别、年龄、门诊或住院病历号、科别或病区和床位号、临床诊断、开具日期等。可添列特殊要求的项目。
麻醉药品和第一类精神药品处方前记:医疗机构名称、费别、患者姓名、性别、年龄、门诊或住院病历号、科别或病区和床位号、临床诊断、开具日期、患者身份证明编号、代办人姓名、身份证明编号。
处方正文:以Rp或R标示:药品名称、剂型、规格、数量、用法用量。
处方后记:医师签名或加盖专用签章、药品金额以及审核、调配、核对、发药药师签名或加盖专用签章。
2、《处方管理办法》规定:药师书写的药袋或粘贴的标签,注明患者姓名和药品名称、用法、用量、包装。
3、GSP规定:药品拆零销售使用的工具、包装应清洁和卫生,出售时应在药袋上写明药品名称、规格、服法、用量、有效期等。
4、医疗机构根据麻醉药品和精神药品处方开具情况,按品种、规格对其消耗量进行专册登记,登记内容包括发药日期、患者姓名、用药数量。专册保存期限为3年。
5、社会保险经办机构与定点零售药店签订协议的内容包括:服务范围、服务内容、服务质量、药费结算办法以及药费审核与控制等。
出国留学网执业药师栏目推荐:
11-11
考试临近,出国留学网定期为你整理执业药师复习要点,与你一起巩固知识点,更多执业药师考试资讯,网站将持续更新,敬请关注!
2017年《药事管理与法规》考点:药品与药品安全
药品与药品安全(2-3分)
1.药品的界定、质量特性和特殊性
(1)药品的界定
《药品管理法》规定,药品是指“用于预防、治疗、诊断人的疾病,有目的地调节人的生理机能并规定有适应症或者功能主治、用法和用量的物质,包括中药材、中药饮片、中成药、化学原料药及其制剂、抗生素、生化药品、放射性药品、血清、疫苗、血液制品和诊断药品等”。
①药品特指人用药品,不包括兽药和农药。
②药品的使用目的、方法有严格规定。使用目的是用于预防、治疗、诊断人的疾病,有目的地调节人的生理机能;使用方法要求必须遵循规定的适应症或者功能主治、用法和用量。
③药品的法定范围包括“中药材、中药饮片、中成药、化学原料药及其制剂、抗生素、生化药品、放射性药品、血清、疫苗、血液制品和诊断药品等”。
可以将药品大致分为三类:
中药:中药材、中药饮片、中成药
化学药:化学原料药及其制剂、抗生素
生物药:包括血清、疫苗、血液制品。
生化药品:我国药品注册分类中只有中药、化学药品、生物制品的分类,没有生化药品的注册类别,因此通常根据药品制造中更多依赖生物技术或化学技术来决定是按生物制品还是按化学药品审批。
④药品不单指药物成品或者药物制剂,也包括原料药物和中药材。
⑤《药品管理法》界定的药品包括诊断药品。诊断药品包括体内使用的诊断药品和按药品管理的用于血源筛査的体外诊断试剂和采用放射性核素标记的体外诊断试剂。其他的更多体外诊断试剂在我国是按医疗器械进行管理的。
(2)药品的质量特性
①有效性:在规定的适应症、用法和用量的条件下,能满足预防、治疗、诊断人的疾病,有目的地调节人的生理机能的要求。有效性是药品的固有特性。若对防治疾病没有效,则不能成为药品。但有效性必须在一定前提条件下产生,即有一定适应症、用法和用量。我国对药品的有效性按在人体达到所规定的效应程度分为“痊愈”、“显效”、“有效”。国际上有的采用“完全缓解”、“部分缓解”、“稳定”来区别。
②安全性:按规定的适应症和用法、用量使用药品后,人体产生毒副反应的程度。大多数药品均有不同程度的毒副反应,只有在衡量有效性大于毒副反应,或可解除、缓解毒副作用的情况下才能使用某种药品。如果某种物质对一些疾病治疗有效,但是对人体有致畸、致癌、甚至致死,那么该物质就不能成为药品。
③稳定性:在规定的条件下保持其有效性和安全性的能力。所谓规定的条件是指在规定的有效期内,以及生产、贮存、运输和使用的条件。如某些物质虽然具有预防、治疗、诊断疾病的...
11-11
考试临近,出国留学网定期为你整理执业药师复习要点,与你一起巩固知识点,更多执业药师考试资讯,网站将持续更新,敬请关注!
2017年《药事管理与法规》考点:执业药师管理
执业药师(6-8分)
(一)执业药师管理
执业药师全国统一考试合格,取得《执业药师资格证书》并经注册登记,在药品生产、经营、使用单位中执业的药学技术人员。
《执业药师资格证书》在全国范围内有效。
(1)执业药师管理部门:
国家食品药品监督管理总局组织考试注册登记和监督管理
人力资源和社会保障部审定会同国家食品药品监督管理总局监督、指导并确定合格标准
执业药师资格考试工作由人力资源和社会保障部与国家食品药品监督管理总局共同负责,日常工作委托国家食品药品监督管理总局执业药师资格认证中心承担,考务工作由人社部人事考试中心负责。考试实行全国统一大纲、统一命题、统一组织。
申请参加执业药师资格考试的人员必须满足以下条件:①中华人民共和国公民和获准在我国境内就业的其他国籍人员。②具有药学、中药学或相关专业中专以上(含中专)学历,并有一定的专业工作实践经历(工作年限)。在报考条件中对专业工作年限的具体规定是,对中专学历的人员要求从事药学或中药学专业工作满七年;对大专学历的人员要求从事药学或中药学专业工作满五年;对本科学历的人员要求从事药学或中药学专业工作满三年;对第二学士学历、研究生班毕业或取得硕士学位的人员要求从事药学或中药学专业工作满一年;取得博士学历的人员可直接申请参加考试。
按照国家有关规定评聘为高级专业技术职务,具备“中药学徒、药学或中药学专业中专毕业,连续从事药学或中药学专业工作满20年”,或者“取得药学、中药学专业或相关专业大专以上学历,连续从事药学或中药学专业工作满15年”条件之一者,可免试部分考试科目。
(2)执业药师注册管理:我国执业药师实行注册制度,取得执业药师资格的药学人员,经执业单位同意,并按规定完成继续教育,到执业单位所在省级执业药师注册机构办理注册手续。取得《执业药师注册证》后,方可以执业药师身份执业。凡持有《执业药师资格证书》而未经注册的人员,不得从事执业药师执业活动。
国家食品药品监督管理总局为全国执业药师注册管理机构,各省级食品药品监督管理部门为本辖区执业药师注册机构。执业药师应当按照执业类别、执业范围、执业地区到执业单位所在省级执业药师注册机构进行注册。执业类别为药学类、中药学类、药学与中药学类;执业范围为药品生产、药品经营、药品使用。机关、院校、科研单位、药品检验机构不属于执业单位,不予注册;执业地区为省、自治区、直辖市。
执业药师只能在一个执业药师注册机构注册,在一个执业单位按照注册的执业类别、执业范围执业。如执业范围为药品经营,则需在《执业药师注册证》上注明药品经营(批发)或药品经营(零售);如注册在零售连锁企业,则应在《执业药师注册证》上注明药品经营(零售),注册的执业单位应当明确到总部或门店,执业药师应当在其注册的执业单位执业。
11-10
考试临近,出国留学网定期为你整理执业药师复习要点,与你一起巩固知识点,更多执业药师考试资讯,网站将持续更新,敬请关注!
2017年《药事管理与法规》考点:特殊管理的药品管理
国家对麻醉药品、精神药品、医疗用毒性药品、放射性药品,实行特殊管理。*
国家对预防性生物制品的流通实行特殊管理*
国家食品药品监督管理部门对药品类易制毒化学品,实施一定的特殊管理;对兴奋剂药品,依其品种不同实施不同层次的管理。
麻醉药品和精神药品的管理(3-4分)
1.概述
麻醉药品、精神药品的概念
麻醉药品是指连续使用后易产生身体 依赖性、能成瘾癖的药品。 *
精神药品精神药品是指直接作用于中枢神经系统,使之兴奋或抑制,连续使用可产生依赖性 的药品。 *
依据精神药品使人体产生的依赖性和危害 人体健康的程度,精神药品分为第一类精神药品和第二类精神药品。 *
麻醉药品与精神药品的专有标志*
麻醉药品专用标志样式(颜色:天蓝色与白色相间* )
精神药品的专用标志样式(颜色:绿色与白色相间* )
麻醉药品和精神药品的管理部门、职责*
(1)国务院药品监督管理部门负责全国麻醉药品和精神药品的监督管理工作,并会同国务院农业主管部门对麻醉药品药用原植物实施监督管理。
省级药品监督管理部门负责本行政区域内麻醉药品和精神药品的监督管理工作。
(2)国务院公安部门负责对造成麻醉药品药用原植物、麻醉药品和精神药品流入非法渠道的行为进行查处。*
县级以上地方公安机关负责对本行政区域内造成麻醉药品和精神药品流入非法渠道的行为进行查处。
(3)卫生部门负责医疗机构内麻醉药品和精神药品的使用管理。 *
2.麻醉药品和精神药品目录:我国生产和使用的麻醉药品和精神药品品种*
麻醉药品和精神药品目录由国务院药品监督管理部门会同国务院公安部门、国务院卫生主管部门制定、调整并公布。 *
《麻醉药品品种目录(2013版)》共121个品种,其中我国生产及使用的品种及包括的制剂、提取物、提取粉共有27个品种,具体有以下品种。
(1)可卡因*
(2)罂粟秆浓缩物(包括罂粟果提取物、罂粟果提取物粉)
(3)二氢埃托啡*
(4)地芬诺酯*
(5)芬太尼*
(6)氢可酮*
(7)氢吗啡酮
(8)美沙酮*
(9)吗啡(包括吗啡阿托品注射液) *
(10)阿片(包括复方樟脑酊、阿桔片) *
(11)羟考酮*
(12)哌替啶*
(13)瑞芬太尼
(14)舒芬太尼
(15)蒂巴因
(16)可待因*
(17)右丙氧芬*
(18)双氢可待因
药事管理与法规复习资料推荐访问