出国留学网专题频道高考化学必考知识点栏目,提供与高考化学必考知识点相关的所有资讯,希望我们所做的能让您感到满意!
高考选了化学的朋友们注意了,小编汇整了高考化学考试必考知识点,为方便您对高考化学考试内容的全面了解,小编从高考化学的考核目标与要求、高考化学的必考知识点和高考化学的选考知识点三个层次来说明此次高考化学大考点内容及考核目标和要求,预祝您考试顺利!!!
必考内容涵盖必修模块"化学1""化学2"和选修模块"化学反B应原理"的内容。根据化学的学科体系和学科特点,必考部分的内容包括:化学学科特点和基本研究方法、化学基本概念和基本理论、常见无机物及其应用、常见有机物及其应用和化学实验基础五个方面。
1.化学学科特点和基本研究方法
(1)了解化学的主要特点是在原子、分子水平上认识物质。了解化学可以识别、改变
和创造分子。
(2)了解科学探究的基本过程,学习运用以实验和推理为基础的科学探究方法。认识
化学是以实验为基础的一门科学。
(3)了解物质的组成、结构和性质的关系。了解化学反应的本质、基本原理以及能量
变化等规律。
(4)了解定量研究方法是化学发展为一门科学的重要标志。了解化学与生活、材料、能源、环境、生命、信息技术等的关系。了解"绿色化学"的重要性。
2.化学基本概念和基本理论
(1)物质的组成、性质和分类
了解分子、原子、离子和原子团等概念的含义。
理解物理变化与化学变化的区别与联系。
理解混合物和纯净物、单质和化合物、金属和非金属的概念。
理解酸、碱、盐、氧化物的概念及其相互联系。
(2)化学用语及常用物理量
熟记并正确书写常见元素的名称、符号、离子符号。
熟悉常见元素的化合价。能根据化合价正确书写化学式(分子式),或根据化学式判断元素的化合价。
掌握原子结构示意图、电子式、分子式、结构式和结构简式等表示方法。
了解相对原子质量、相对分子质量的定义,并能进行有关计算。
理解质量守恒定律。
能正确书写化学方程式和离子方程式,并能进行有关计算。
了解物质的量(n)及其单位摩尔(mol)、摩尔质量(M)、气体摩尔体积(Vm)、
物质的量浓度(c)、阿伏加德罗常数(NA)的含义。
能根据微粒(原子、分子、离子等)物质的量、数目、气体体积(标准状况下)之间的相互关系进行有关计算。
(3)溶液
了解溶液的含义。
了解溶解度、饱和溶液的概念。
了解溶液浓度的表示方法。理解溶液中溶质的质量分数和物质的量浓度的概念,并能进行有关计算。
掌握配制一定溶质质量分数溶液和物质的量浓度溶液的方法。
了解胶体是一种常见的分散系,了解溶液和胶体的区别。
(4)物质结构和元素周期律
了解元素、核素和同位素的含义。
了解原子的构成。了解原子序数、核电荷数、质子数、中子数、核外电子数以及它们之间的相互关系。
了解原子核外电子排布规律。
...
下文是特为2023届高考考生整理的化学考试科目的必考知识点,相信对各位高考生会有很大的帮助,各位考生们快来看看吧!下面是出国留学网整理的“2023年高考科目化学考试必考知识点归纳”,此文本仅供参考,欢迎阅读。
1. 混合物的分离
①过滤:固体(不溶)和液体的分离。
②蒸发:固体(可溶)和液体分离。
③蒸馏:沸点不同的液体混合物的分离。
④分液:互不相溶的液体混合物。
⑤萃取:利用混合物中一种溶质在互不相溶的溶剂里溶解性的不同,用一种溶剂把溶质从它与另一种溶剂所组成的溶液中提取出来。
2. 粗盐的提纯
(1)粗盐的成分:主要是NaCl,还含有MgCl2、CaCl2、Na2SO4、泥沙等杂质
(2)步骤:
①将粗盐溶解后过滤;
②在过滤后得到粗盐溶液中加过量试剂BaCl2(除SO42-)、Na2CO3(除Ca2+、过量的Ba2+)、NaOH(除Mg2+)溶液后过滤;
③得到滤液加盐酸(除过量的CO32-、OH-)调pH=7得到NaCl溶液;
④蒸发、结晶得到精盐。
加试剂顺序关键:Na2CO3在BaCl2之后;盐酸放最后。
(3) 蒸馏装置注意事项:
①加热烧瓶要垫上石棉网;
②温度计的水银球应位于蒸馏烧瓶的支管口处;
③加碎瓷片的目的是防止暴沸;
④冷凝水由下口进,上口出。
(4) 从碘水中提取碘的实验时,选用萃取剂应符合原则:
①被萃取的物质在萃取剂溶解度比在原溶剂中的大得多;
②萃取剂与原溶液溶剂互不相溶;
③萃取剂不能与被萃取的物质反应。
3. 离子的检验
①SO42-:先加稀盐酸,再加BaCl2溶液有白色沉淀,原溶液中一定含有SO42-。Ba2++SO42-=BaSO4↓
②Cl-(用AgNO3溶液、稀硝酸检验)加AgNO3溶液有白色沉淀生成,再加稀硝酸沉淀不溶解,原溶液中一定含有Cl-;或先加稀硝酸酸化,再加AgNO3溶液,如有白色沉淀生成,则原溶液中一定含有Cl-。Ag++Cl-=AgCl↓。
③CO32-:(用BaCl2溶液、稀盐酸检验)先加BaCl2溶液生成白色沉淀,再加稀盐酸,沉淀溶解,并生成无色无味、能使澄清石灰水变浑浊的气体,则原溶液中一定含有CO32-。
4. 5个新的化学符号及关系
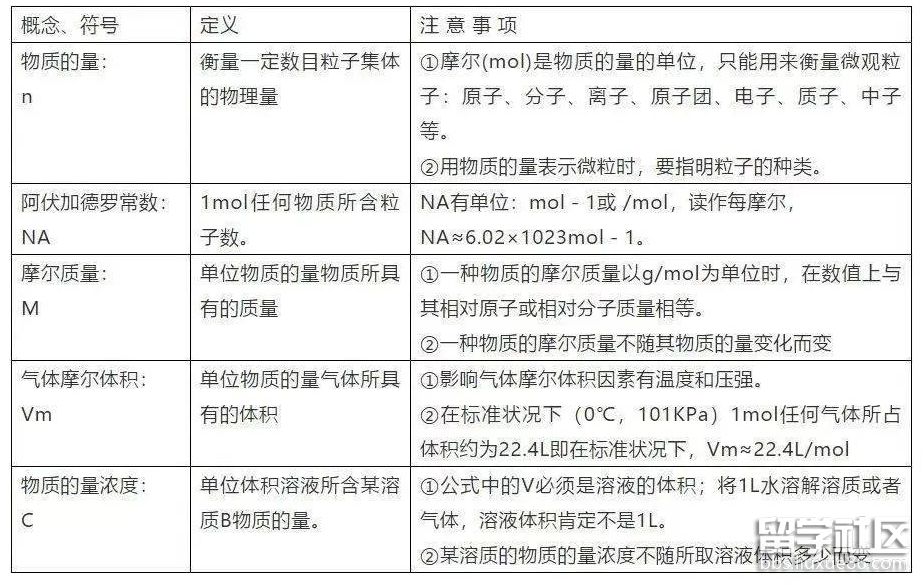
有些人说高考化学是理科中的文科,说明高考化学需要记住的东西很多。为了帮助大家更好的复习。下面是由出国留学网小编为大家整理的“高考化学必考知识点总结”,仅供参考,欢迎大家阅读。
高考化学知识点总结
1、有色气体:F2(淡黄绿色)、Cl2(黄绿色)、Br2(g)(红棕色)、I2(g)(紫红色)、NO2(红棕色)、O3(淡蓝色),其余均为无色气体。其它物质的颜色见会考手册的颜色表。
2、有刺激性气味的气体:HF、HCl、HBr、HI、NH3、SO2、NO2、F2、Cl2、Br2(g);有臭鸡蛋气味的'气体:H2S。
3、熔沸点、状态:
① 同族金属从上到下熔沸点减小,同族非金属从上到下熔沸点增大。
② 同族非金属元素的氢化物熔沸点从上到下增大,含氢键的NH3、H2O、HF反常。 ③ 常温下呈气态的有机物:碳原子数小于等于4的烃、一氯甲烷、甲醛。
④ 熔沸点比较规律:原子晶体>离子晶体>分子晶体,金属晶体不一定。
⑤ 原子晶体熔化只破坏共价键,离子晶体熔化只破坏离子键,分子晶体熔化只破坏分子间作用力。
⑥ 常温下呈液态的单质有Br2、Hg;呈气态的单质有H2、O2、O3、N2、F2、Cl2;常温呈液态的无机化合物主要有H2O、H2O2、硫酸、硝酸。
⑦ 同类有机物一般碳原子数越大,熔沸点越高,支链越多,熔沸点越低。
同分异构体之间:正>异>新,邻>间>对。
⑧ 比较熔沸点注意常温下状态,固态>液态>气态。如:白磷>二硫化碳>干冰。
⑨ 易升华的物质:碘的单质、干冰,还有红磷也能升华(隔绝空气情况下),但冷却后变成白磷,氯化铝也可;三氯化铁在100度左右即可升华。
⑩ 易液化的气体:NH3、Cl2 ,NH3可用作致冷剂。
高考化学知识要点
一、溶解性
① 常见气体溶解性由大到小:NH3、HCl、SO2、H2S、Cl2、CO2。极易溶于水在空气中易形成白雾的气体,能做喷泉实验的气体:NH3、HF、HCl、HBr、HI;能溶于水的气体:CO2、SO2、Cl2、Br2(g)、H2S、NO2。极易溶于水的气体尾气吸收时要用防倒吸装置。
② 溶于水的有机物:低级醇、醛、酸、葡萄糖、果糖、蔗糖、淀粉、氨基酸。苯酚微溶。 ③ 卤素单质在有机溶剂中比水中溶解度大。
④ 硫与白磷皆易溶于二硫化碳。
⑤ 苯酚微溶于水(大于65℃易溶),易溶于酒精等有机溶剂。
⑥ 硫酸盐三种不溶(钙银钡),氯化物一种不溶(银),碳酸盐只溶钾钠铵。
⑦ 固体溶解度大多数随温度升高而增大,少数受温度影响不大(如NaCl),极少数随温度升高而变小[如Ca(OH)2]。 气体溶解度随温度升高而变小,随压强增大而变大。
二、密度
① 同族元素单质一般密度从上到下增大。
② 气体密度大小由相对分子质量大小决定。
③ 含C、H、O的有机物一般密度小于水(苯酚大于水),含溴、碘、硝基、多个氯的有机物密度大于水。
④ 钠的密度小于水,大于酒精、苯。
高考化学知识点
...
高考化学必考的理论知识有哪些?需要了解的考生看过来,下面由出国留学网小编为你精心准备了“高考化学必考知识点有哪些”仅供参考,持续关注本站将可以持续获取更多的内容!
1、氧化还原相关概念和应用
(1)借用熟悉的H2还原CuO来认识5对相应概念。
(2)氧化性、还原性的相互比较。
(3)氧化还原方程式的书写及配平。
(4)同种元素变价的氧化还原反应(歧化、归中反应)。
(5)一些特殊价态的微粒如H、Cu、Cl、Fe、S2O32–的氧化还原反应。
(6)电化学中的氧化还原反应。
2、物质结构、元素周期表的认识
(1)主族元素的阴离子、阳离子、核外电子排布。
(2)同周期、同主族原子的半径大小比较。
(3)电子式的正确书写、化学键的形成过程、化学键、分子结构和晶体结构。
(4)能画出短周期元素周期表的草表,理解“位—构—性”。
3、熟悉阿伏加德罗常数NA常考查的微粒数止中固体、得失电子、中子数等内容。
4、热化学方程式的正确表达(状态、计量数、能量关系)
5、离子的鉴别、离子共存
(1)离子因结合生成沉淀、气体、难电离的弱电解质面不能大量共存。
(2)因相互发生氧化还原而不能大量共存。
(3)因双水解、生成络合物而不能大量共存。
(4)弱酸的酸式酸根离子不能与强酸、强碱大量共存。
(5)题设中的其它条件:“酸碱性、颜色”等。
6、溶液浓度、离子浓度的比较及计算
(1)善用微粒的守恒判断(电荷守衡、物料守衡、质子守衡)。
(2)电荷守恒中的多价态离子处理。
7、pH值的计算
(1)遵循定义(公式)规范自己的计算过程。
(2)理清题设所问的是“离子”还是“溶液”的浓度。
(3)酸过量或碱过量时pH的计算(酸时以H+浓度计算,碱时以OH–计算再换算)。
8、化学反应速率、化学平衡
(1)能计算反应速率、理解各物质计量数与反应速率的关系。
(2)理顺“反应速率”的“改变”与“平衡移动”的“辩证关系”。
(3)遵循反应方程式规范自己的“化学平衡”相关计算过程。
(4)利用等效平衡”观点来解题。
9、电化学
(1)能正确表明“原电池、电解池、电镀池”及变形装置的电极位置。
(2)能写出各电极的电极反应方程式。
(3)了解常见离子的电化学放电顺序。
(4)能准确利用“得失电子守恒”原则计算电化学中的定量关系。
10、盐类的水解
(1)盐类能发生水解的原因。
(2)不同类型之盐类发生水解的后果(酸碱性、浓度大小等)。
(3)盐类水解的应用或防止(胶体、水净化、溶液制备)。
(4)对能发生水解的盐类溶液加热蒸干、灼烧的后果。
(5)能发生完全双水解的离子反应...
05-18
口诀记忆
由于知识点多,记忆量大,在化学学习中往往会出现一些很容易记住的口诀,老师要求我们去记忆它。首先,要告诉自己这是一种学习的捷径,然后在深刻的理解它的内涵,最后记住了,就会成为你学习化学的利器。如:“升失氧,降得还”、“见量化摩,求啥先求摩”、“有弱才水解,都强不水解。谁弱谁水解,谁强显谁性。越热越水解,越弱越水解”。
趣味记忆
为了分散难点,提高兴趣,要采用趣味记忆方法来记忆有关的化学知识。比如,可以把生边的实际生活甚至自己的经历和观雪有关知识联系起来,让化学知识富有趣味。特别是一些物质的物理性质和化学反应的现象。
重复记忆
要利用必要的重复来加深记忆事物的印象也是跟遗忘作斗争的有效方法,所以在记住某些知识时常常用默默重复、叙述再现方法来加深印象。这种方法往往被我们忽视了,很多同学学的快忘得快也就是这个原因。短时记忆对于我们的学习远远不够,只有通过不断反复记忆,才能够把短时记忆转化为长时记忆,为我们的学习打下坚实的基础。
归类记忆
对所学知识进行系统分类,抓住特征,在以此类推。如:电解质判断的时候,把所学的化合物归类,再把强电解质弱、电解质的包含的类别记住,对于我们掌握本质就很有帮助;再如:在掌握了各个主族、周期的相似性和递变性规律后,对于具体的元素单质、化合物的性质就容易多了。
对比记忆
对新旧知识中具有相似性和对立性的有关知识进行比较,找出异同点。比如:中学化学中常见的黄色粉末并不多见,主要就是硫磺和过氧化钠,但是它们的性质却很不相同。再如:我们在学习硫酸和硝酸的时候,他们作为氧化性酸的酸性和强氧化性的方面的相似性。
联想记忆
把性质相同、相近、相反的事物特征进行比较,记住他们之间的区别联系,再回忆时,只要想到一个,便可联想到其他。如:记酸、碱、盐的溶解性规律,孤立地记忆很难,如果扩大联想,对比类推,效果可能要好得多。
关键字词记忆
这是记忆概念有效方法之一,在理解基础上找出概念中几个关键字或词来记忆整个概念,如:化学平衡的特征“逆、等、定、动、变”。
知识网络记忆
用表格或图示进行归纳、整理,使看似零散的知识结成网络。如以一主族代表元素的单质、氧化物、氧化物的水化物、盐为线索的学习思路,以及以结构、物理性质、化学性质、用途、制备、保存之间相互关联的元素化合物类知识,在有机中还要特别注意官能团的性质。
需要注意的是,化学中常常有些个别物质性质特殊,这些特殊性最好同类似的对比起来记忆,这一点有时候在解题过程中很重要。不管怎么样,只要能用合适的方法是自己最高效、最牢固的记住并理解所学知识,那么我们的学习就变得轻松有趣了。
推荐阅读:
03-24
2015高考化学必考知识点总结
一、物理性质
1、有色气体:F2(淡黄绿色)、Cl2(黄绿色)、Br2(g)(红棕色)、I2(g)(紫红色)、NO2(红棕色)、O3(淡蓝色),其余均为无色气体。其它物质的颜色见会考手册的颜色表。
2、有刺激性气味的气体:HF、HCl、HBr、HI、NH3、SO2、NO2、F2、Cl2、Br2(g);有臭鸡蛋气味的气体:H2S。
3、熔沸点、状态:
① 同族金属从上到下熔沸点减小,同族非金属从上到下熔沸点增大。
② 同族非金属元素的氢化物熔沸点从上到下增大,含氢键的NH3、H2O、HF反常。
③ 常温下呈气态的有机物:碳原子数小于等于4的烃、一氯甲烷、甲醛。
④ 熔沸点比较规律:原子晶体>离子晶体>分子晶体,金属晶体不一定。
⑤ 原子晶体熔化只破坏共价键,离子晶体熔化只破坏离子键,分子晶体熔化只破坏分子间作用力。
⑥ 常温下呈液态的单质有Br2、Hg;呈气态的单质有H2、O2、O3、N2、F2、Cl2;常温呈液态的无机化合物主要有H2O、H2O2、硫酸、硝酸。
⑦ 同类有机物一般碳原子数越大,熔沸点越高,支链越多,熔沸点越低。
同分异构体之间:正>异>新,邻>间>对。
⑧ 比较熔沸点注意常温下状态,固态>液态>气态。如:白磷>二硫化碳>干冰。
⑨ 易升华的物质:碘的单质、干冰,还有红磷也能升华(隔绝空气情况下),但冷却后变成白磷,氯化铝也可;三氯化铁在100度左右即可升华。
⑩ 易液化的气体:NH3、Cl2 ,NH3可用作致冷剂。
4、溶解性
① 常见气体溶解性由大到小:NH3、HCl、SO2、H2S、Cl2、CO2。极易溶于水在空气中易形成白雾的气体,能做喷泉实验的气体:NH3、HF、HCl、HBr、HI;能溶于水的气体:CO2、SO2、Cl2、Br2(g)、H2S、NO2。极易溶于水的气体尾气吸收时要用防倒吸装置。
② 溶于水的有机物:低级醇、醛、酸、葡萄糖、果糖、蔗糖、淀粉、氨基酸。苯酚微溶。
③ 卤素单质在有机溶剂中比水中溶解度大。
④ 硫与白磷皆易溶于二硫化碳。
⑤ 苯酚微溶于水(大于65℃易溶),易溶于酒精等有机溶剂。
⑥ 硫酸盐三种不溶(钙银钡),氯化物一种不溶(银),碳酸盐只溶钾钠铵。
⑦ 固体溶解度大多数随温度升高而增大,少数受温度影响不大(如NaCl),极少数随温度升高而变小[如。 气体溶解度随温度升高而变小,随压强增大而变大。
5、密度
① 同族元素单质一般密度从上到下增大。
② 气体密度大小由相对分子质量大小决定。
③ 含C、H、O的有机物一般密度小于水(苯酚大于水),含溴、碘、硝基、多个氯的有机物密度大于水。
④ 钠的...
高考化学必考知识点
1、各种化学用语(核素、离子、原子的标记符号;各种化学式、方程式;结构简式、结构式;分子式、最简式、实验式-------)
2、原子、离子的结构特征(各电子层结构、最外层电子数、半径)及性质(得失电子能力、氧化还原性)
3、周期律的内涵(原子离子结构的周期性变化、原子离子得失电子能力的周期性变化、元素金属性和非金属性的周期性变化、元素单质的性质的周期性变化、元素化合物的性质的周期性变化)
4、周期表的结构及构成规律
5、反应速率的计算(表示、比较、换算------)及影响反应速率的各种因素(要求识别图像和绘制图像)
6、平衡状态的特征与判断、平衡移动的判断(从浓度、转化率、体积百分含量、平均相对分子质量、密度、压强、-------)
7、有关化学平衡常数的简单计算
8、弱电解质(含水)的电离平衡移动的分析
9、溶液的酸碱性、pH(PH试纸及PH计的使用)及简单计算、指示剂
10、盐的水解的本质及表示方法
11、离子反应的本质、离子共存的分析、离子浓度的大小比较
12、关于氧化还原反应(无机、有机)的分析、简单的配平与基本计算
13、关于电化学(原电池、电解池)的分析
14、反应热、热化学方程式、盖斯定律及应用
15、同分异构体的分析与判断
16、重要官能团的结构、典型反应及相互转化
17、有机反应类型及典型例证
18、有机物的合成与推断
19、以氯气、氯水、次氯酸及其盐、漂白粉为线索的卤族元素
20、以二氧化硫、浓硫酸为线索的氧族元素
21、以氮的氧化物,硝酸,氨气,氨水,铵盐为线索的氮族元素
22、以硅及其氧化物为线索的碳族元素
23、以钠及过氧化钠为主线的碱金属元素
24、铝、氧化铝、铝盐及偏铝酸盐
25、二价铁和三价铁的相互转化及应用
26、教材上的演示实验(目的、原理、装置、操作、现象、拓展-------)
27、做过的分组实验(目的、原理、装置、操作、现象、评价、改进-----)
28、相关概念——电离、电解、电镀、电池、电泳、电化腐蚀、电极、原电池、电解池
29、相反概念——阴极和阳极,正极和负极,加成和消去,氧化反应和还原反应
30、相似概念——同位素、同素异形体、同分异构体、同系物和同系列,挥发和升华
31、相近概念——核素、同位素和元素,原子的性质、元素的性质和单质的性质,原子的质量、原子的相对原子质量、元素的相对原子质量和质量数。
出国留学网高考频道为您整理史上高考复习资料大全!让您的高考成绩稳步上升...
同学们要走出“越基础的东西越易出差错”的怪圈,除了要在思想上重视外,还得对作业、考试中出现的差错,及时反思,及时纠正;对“事故易发地带”有意识地加以强化训练是一条有效的途径。更多有关2014高考理综的信息可登录出国留学网理综频道,欢迎收藏本站(CTRL+D即可收藏)!

| 2014试题库汇总 | ||
|---|---|---|
| 5年高考3年模拟汇总 | 每日一练(72套含答案) | 2014高考语言运用汇总 |
| ... | ||
高考化学必考知识点推荐访问